Coito programado – Indução da ovulação
Nos tratamentos de coito programado (baixa complexidade), a fertilização ocorre no próprio organismo e não necessita de uma estrutura de laboratório complexa nem ambiente cirúrgico para sua realização. Além disso, utilizam protocolos simples e de baixo risco para estimulação ovariana, sendo mais fáceis de ser realizados pelo ginecologista geral.
Já na alta complexidade, a fertilização ocorre no laboratório, por isso chamamos fertilização in vitro (FIV), necessitando de um equipamento laboratorial sofisticado além de envolver protocolos mais complexos de estimulação ovariana.
Para definirmos o melhor tratamento é importante uma avaliação completa do casal para saber se devemos começar por algo mais simples ou se seria indicado ir direto para o de alta complexidade. Isso se justifica, pois, qualquer tratamento, por mais simples que seja, envolve desgaste emocional e frustração se o resultado for negativo. Assim, é necessária uma pesquisa mínima da fertilidade antes da indicação de um determinado trata¬mento para que não se insista em uma opção com baixa chance de sucesso.
Quais os exames mínimos necessários?
Índice
Toggle1. Espermograma completo;
2. Histerossalpingografia ou videolaparoscopia;
3. Ultrassonografia endovaginal;
4. Dosagens hormonais – FSH e LH (do 3º ao 5º dia do ciclo), TSH, T4 livre e prolactina;
5. Avaliação da reserva ovariana;
6. Sorologias do casal
Os principais requisitos que determinam a possibilidade de tratamento de baixa complexidade são:
• permeabilidade tubária (comprovada por histerossalpingografia ou laparoscopia);
• espermograma com morfologia normal e processamento seminal com mais de cinco milhões de espermatozoides móveis.
Nos casos em que estes requisitos não forem preenchidos, recomenda-se, com o entendimento e consentimento do casal, a indicação da FIV. Há ainda outros fatores que não são excludentes de um tratamento de baixa complexidade, mas muito importantes na decisão: idade, tempo de infertilidade e fatores de infertilidade associados. Idade maior que 37 anos, tempo de infertilidade maior que cinco anos, reserva ovariana baixa e endometriose moderada/grave são mau prognóstico para baixa complexidade, assim esses casos devem ser avaliados criteriosamente, um a um. Não se deve esquecer ainda que pesam nessa decisão: a ansiedade, a vontade e a disponibilidade financeira do casal.
COITO PROGRAMADO OU “NAMORO” PROGRAMADO (BAIXA COMPLEXIDADE)
O coito programado é a determinação do melhor período do ciclo menstrual para o casal ter relações sexuais e conseguir a gestação, utilizando-se o conhecimento médico e a tecnologia. Ele pode ser em ciclo natural ou com medicamentos indutores da ovulação. As principais indicações do coito programado são:
• pacientes jovens (abaixo de 37 anos);
• pacientes com fator ovulatório como única causa de infertilidade;
• virgens de tratamentos anteriores;
• qualidade adequada do sêmen;
• integridade anatômica do sistema reprodutor feminino.
Que conhecimentos e recursos são necessários para realizar o coito programado?
1. conhecimento sobre as drogas e as complicações dos esquemas de indução da ovulação;
2. ultrassom endovaginal;
3. se for possível, um laboratório à disposição, para dosagem rápida de hormônios.
COITO PROGRAMADO PASSO A PASSO
Estimulação ovariana
A estimulação ovariana é uma etapa importante para o sucesso do tratamento de Coito Programado. Tem o objetivo de estimular mais de um oócito, dois ou três no máximo, para que se aumente a taxa de um resultado positivo, pela quantidade e a qualidade dos oócitos produzidos.
Muitos estudos têm demonstrado os benefícios da estimulação ovariana quando comparados aos ciclos espontâneos. A taxa de gravidez sem estimulação ovariana é muita baixa, tanto no coito programado (cerca de 1,5%) quanto na inseminação (cerca de 4%). Comparando-se as taxas de gravidez entre grupos de pacientes que tiveram os ovários estimulados com outras que não tiveram, foram encontradas taxas de gestação até cinco vezes maior no grupo que recebeu o estímulo.
Para a estimulação ovariana, é importante que o ginecologista não só tenha conhecimento dos medicamentos utilizados na rotina deste procedimento, como também realize exames de ultrassom para o acompanhamento do desenvolvimento folicular. Se o profissional não tiver este recurso, deverá ter parceria com uma clínica de ultrassom experiente que possa avaliar o ciclo ovulatório desde o início da menstruação. O primeiro exame deverá ocorrer no 2º ou 3º dia da menstruação para que se confirme a inexistência de folículos remanescentes do ciclo anterior, e depois deve ser repetido de acordo com o desenvolvimento folicular, até que se obtenha pelo menos um folículo com o diâmetro médio de 18 mm e o endométrio com espessura superior a 7 mm. Um laboratório de análises clínicas que entregue em poucas horas o resultado de dosagens hormonais de estradiol e progesterona pode ser útil nas situações em que houver dúvidas quanto à real fase do ciclo ovulatório ou se a ovulação ocorreu antes do período previsto. Quando isso ocorrer, deve ser ponderado o cancelamento do procedimento.
A indução da ovulação pode utilizar vários diferentes medicamentos, orais ou injetáveis, isolados ou em associação. Os principais esquemas são:
a. Citrato de clomifeno
É o fármaco mais usado nas induções de ovulação desde 1965. A dose é de 50 a 150mg/dia por cinco dias, iniciando entre o 2º e o 5º dia do ciclo. Normalmente começamos com 50 mg ao dia e, se não houver resposta, aumentamos para 100 e 150 mg/d (Quadro 6-1). O citrato de clomifeno tem as grandes vantagens de ser via oral e de baixo custo. Entretanto, apresenta algumas desvantagens devido à sua ação antiestrogênica no útero, levando ao antagonismo do estrógeno no endométrio e no muco cervical, prejudicando-os. Além disso, quando comparado às gonadotrofinas injetáveis, desenvolve menos folículos.
b. Tamoxifeno
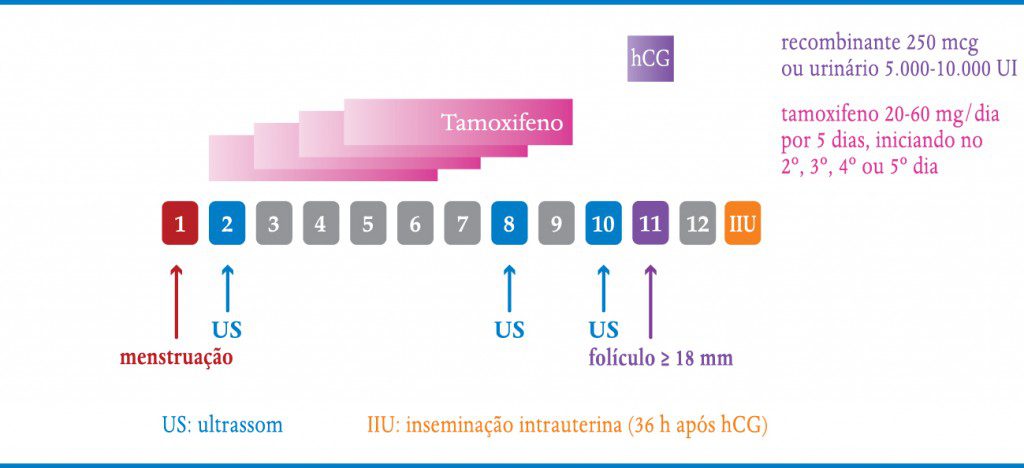
É um SERM (selective estrogen receptor modulator), ou seja, um modulador seletivo do receptor de estrógeno, podendo ter efeito agonista ou antagonista, dependendo do órgão. Como no hipotálamo e na hipófise tem efeito antagonista, tem ação semelhante ao citrato de clomifeno. A vantagem é que nos receptores de estrógeno do útero, o tamoxifeno tem efeito agonista, não prejudicando o endométrio e o muco cervical, como o clomifeno. Não é muito utilizado na prática. A dose recomendada é 20 a 60 mg/d por cinco dias, iniciando entre o 2º e o 5º dia do ciclo (Quadro 6-2).
c. Inibidor de aromatase (Anastrozole e Letrozole)
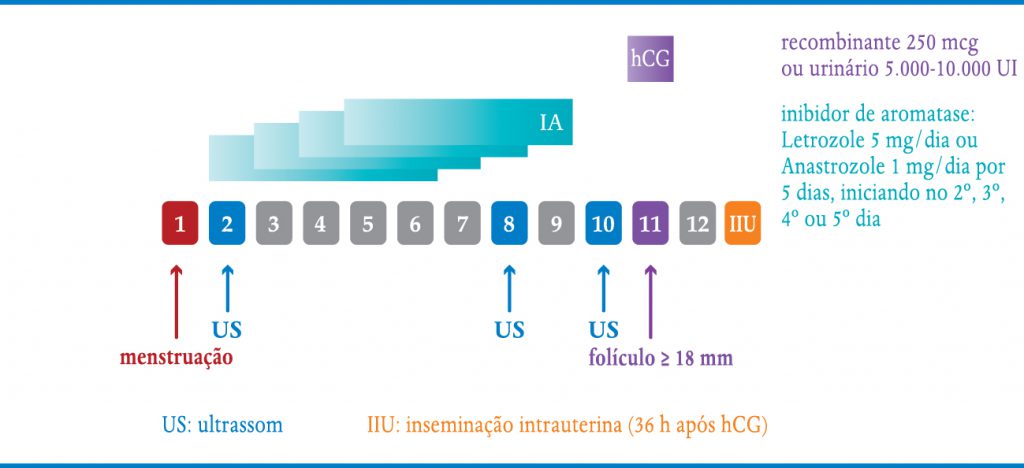
Em geral, leva a uma resposta monofolicular. Tem a vantagem sobre o clomifeno de não ter os efeitos negativos sobre o muco cervical e o endométrio. É uma opção para as pacientes resistentes ao citrato de clomifeno ou que apresentaram endométrio fino (< 7 mm) com seu uso. A dose é 5 mg/dia de letrozole ou 2 mg/dia de anastrozole por cinco dias, iniciando entre o 2º e o 5º dia do ciclo (Quadro 6-3).
d. Gonadotrofinas injetáveis
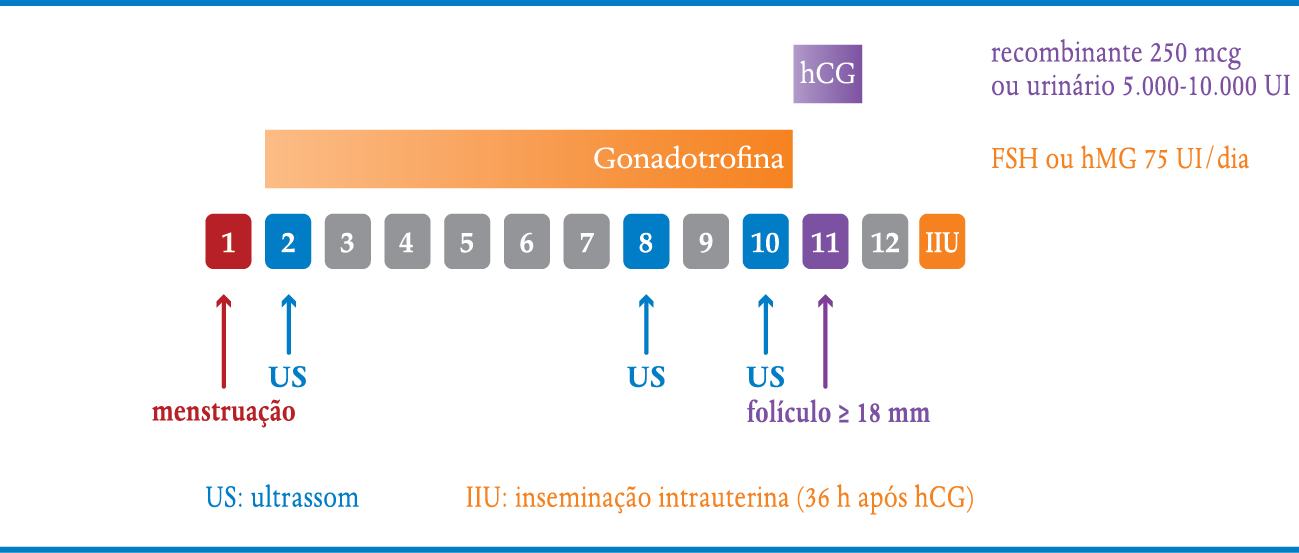
Podem ser derivadas de urina de mulheres menopausadas, como o FSH isolado ou com componente LH (hMG), ou sintetizadas por engenharia genética, como o FSH recombinante. As gonadotrofinas têm a desvantagem de ter um custo elevado e ser de uso subcutâneo. Mas em geral levam ao crescimento de mais folículos e têm melhores taxas de sucesso. A dose é geralmente de 75 UI em dias alternados (ou diária), iniciando-se no 2º ou 3º dia do ciclo (Quadro 6-4). Não há diferença entre as variadas gonadotrofinas injetáveis em termos de eficácia de um modo geral. Nas pacientes com Síndrome dos Ovários Policísticos, a utilização de FSH isolado costuma ter melhores resultados, uma vez que estas apresentam níveis elevados de LH. Em mulheres com hipogonadismo hipogonadotrópico, como há déficit de produção endógena de gonadotrofinas, o indutor oral não tem resposta, sendo necessárias gonadotrofinas injetáveis, de preferência com componente LH associado (hMG). As urinárias têm ainda a vantagem de ser mais baratas.
e. Esquemas mistos
Algumas vezes podemos associar um dos indutores via oral com gonadotrofinas injetáveis, em diferentes esquemas (Quadro 6-5 e 6-6).
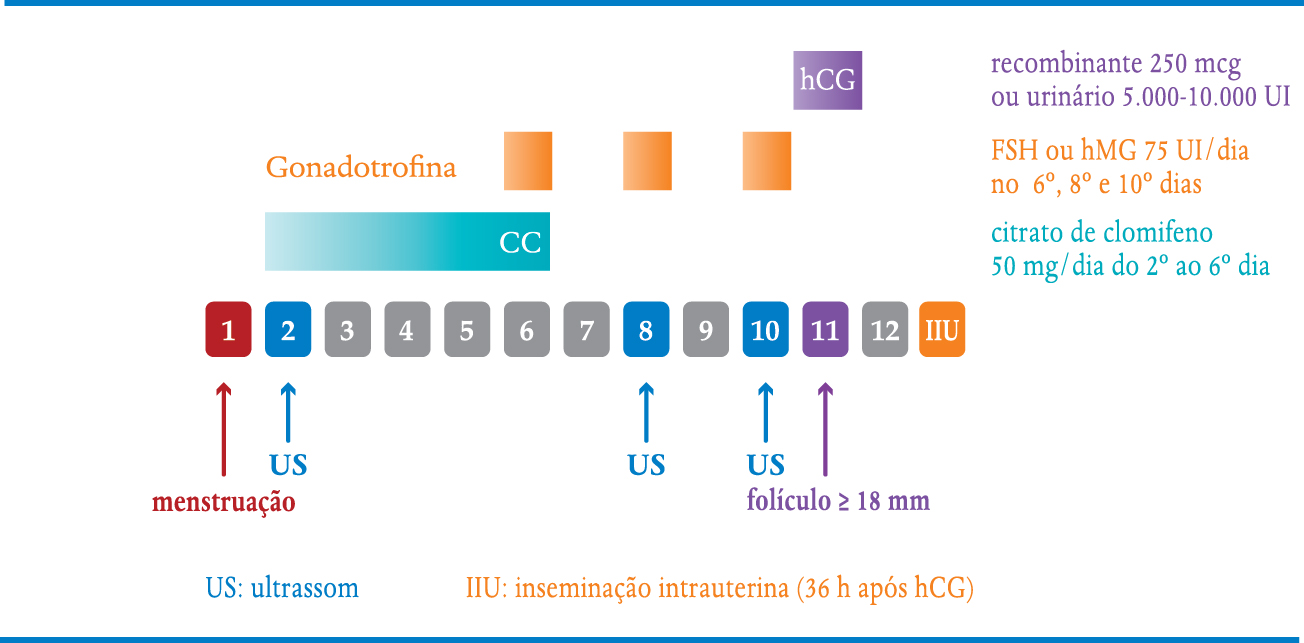
Os tratamentos iniciam-se entre o 2º e o 5º dia do ciclo menstrual com a realização de uma ultrassonografia transvaginal para a avaliação ovariana, verificação da existência de cistos remanescentes, reserva ovariana e checagem do endométrio (Figura 6-1). A partir daí inicia-se ou não a indução da ovulação. Por volta do 8º dia do ciclo, a paciente retorna para controle ultrassonográfico seriado a cada dois dias, até a obtenção de um ou mais folículos (três no máximo) com 18 mm de diâmetro médio (Figura 6-2 e 6-3). Caso haja mais de três folículos maiores que 16 mm, o ciclo deve ser suspenso e a paciente orientada a ter relações com preservativo, pelo risco de gravidez múltipla. Outra possibilidade é converter o ciclo em um de fertilização in vitro. É importante também avaliar a espessura endometrial. Caso o endométrio não ultrapasse 7 mm, o que ocorre principalmente com o uso do clomifeno, também vale a pena suspender o ciclo e trocar a estimulação ovariana para inibidores de aromatase ou gonadotrofinas injetáveis.
FIGURA 6-1. ULTRASSOM NO 2º – 3º DIA DO CICLO MENSTRUAL PARA INICIAR ESTIMULAÇÃO OVARIANA PARA COITO PROGRAMADO OU INSEMINAÇÃO INTRAUTERINA
Observa-se endométrio fino (< 5 mm) e ausência de folículos ovarianos > 10 mm.

FIGURA 6-2. ULTRASSOM DE 8º DIA DO CICLO MENSTRUAL COM ESTIMULAÇÃO OVARIANA PARA COITO PROGRAMADO OU INSEMINAÇÃO INTRAUTERINA
Observa-se endométrio tornando-se mais espesso e de aspecto trilaminar e ovários com três folículos em crescimento.
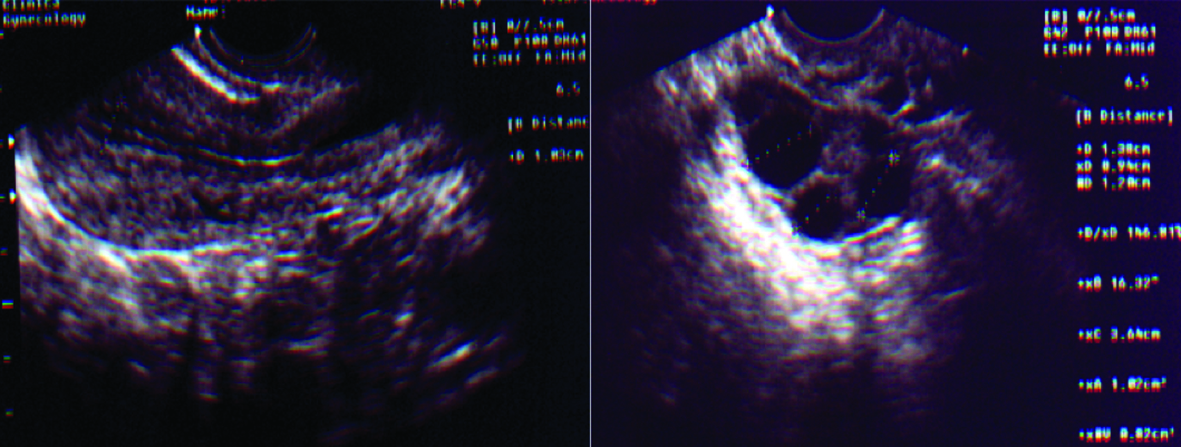
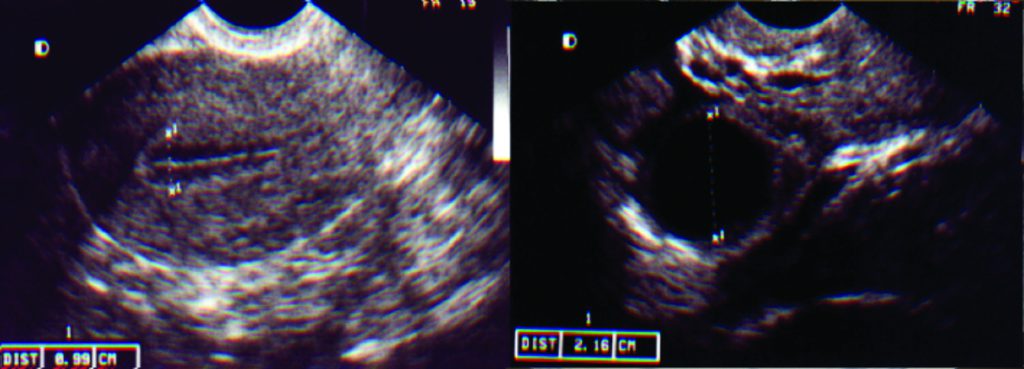
FIGURA 6-3. ULTRASSOM DE 10º DIA DO CICLO MENSTRUAL
COM ESTIMULAÇÃO OVARIANA PARA COITO PROGRAMADO OU INSEMINAÇÃO INTRAUTERINA
Observa-se endométrio de padrão trilaminar com espessura > 7 mm e presença de folículo pré-ovulatório >18 mm
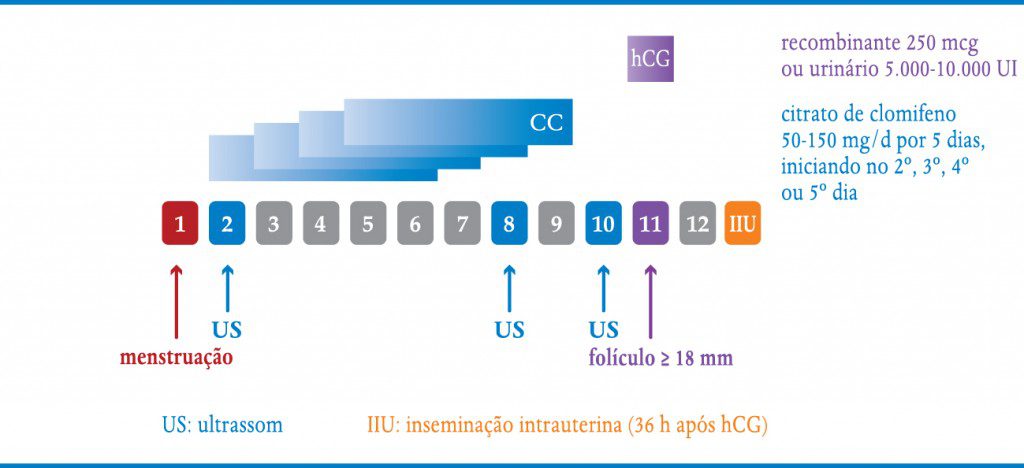
Pico de LH
Quando o maior folículo atinge mais de 18 mm, em ciclos de coito programado, podemos aguardar ocorrer o pico espontâneo de LH ou simular este pico através da utilização da gonadotrofina coriônica ou hCG, que se une aos receptores de LH com ação semelhante deste hormônio. A vantagem de sua utilização é garantir a ovulação, pois nem sempre o pico de LH ocorre. Além disso sabemos o momento em que a paciente irá ovular (36 horas após seu uso). Nos ciclos de inseminação sempre utilizamos para poder programar a hora da inseminação, que pode ser de 24 a 48 horas após sua aplicação. Em pacientes com hipo-gonadismo hipogonadotrópico também é sempre necessário, uma vez que a paciente é incapaz de desencadear o pico endógeno de LH. A dose recomendada é 5.000 UI do hCG urinário ou 250 mcg (1 ampola) do hCG recombinante.
A inseminação intrauterina
Nos casais realizando coito programado, após o hCG, orienta-se que tenham relações sexuais diariamente ou em dias alternados. Nos casais que irão realizar a inseminação intrauterina, em geral ela acontece 36 horas após o hCG. Alguns autores mostraram bons resultados com a inseminação dupla com 12 e 36 horas após a aplicação do hCG.
Para a inseminação uterina é necessário o preparo seminal. A coleta pode ser feita em casa (neste caso a amostra tem que estar no laboratório no máximo 45 minutos após a coleta) ou no laboratório. A coleta é realizada por masturbação e armazenada diretamente em um frasco, que deve ser identificado.
Suporte de fase lútea
Para o suporte de fase lútea, pode-se usar a progesterona ou o hCG. No mercado existem diferentes formas de apresentação da progesterona (oral, vaginal, injetável), não havendo diferenças significativas entre elas. Normalmente, utilizamos 200 mg de progesterona micronizada (utrogestan ou evocanil) via vaginal. Quando comparada ao hCG (utilizado em 1.500 UI a cada três dias), a progesterona apresenta menor risco de hiperestímulo.
Orienta-se o teste de gravidez 14 dias após a inseminação intrauterina ou 16 dias após o hCG, no coito programado.
ALGUNS EXEMPLOS DE PROTOCOLOS DE ESTIMULAÇÃO OVARIANA PARA COITO PROGRAMADO
QUADRO 6-1. CITRATO DE CLOMIFENO
QUADRO 6-2. TAMOXIFENO
QUADRO 6-3. INIBIDOR DE AROMATASE
QUADRO 6-4. GONADOTROFINAS INJETÁVEIS
QUADRO 6-5. CITRATO DE CLOMIFENO + GONADOTROFINAS INJETÁVEIS I
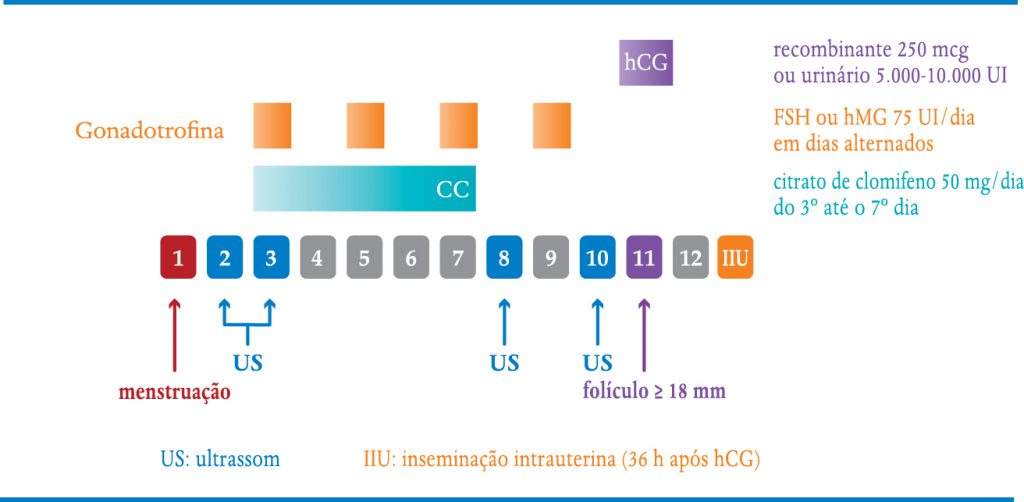
QUADRO 6-6. CITRATO DE CLOMIFENO + GONADOTROFINAS INJETÁVEIS II
COMPLICAÇÕES
Complicações são raras neste tipo de procedimento. Mas, dentre as possibilidades, existe um risco muito baixo de infecção (0,2%), reação alérgica e síndrome do hiperestimulação ovariana (1% a 2%) (Capítulo 10). A principal complicação é a gestação múltipla (16%) quando utilizamos medicamentos para estimulação ovariana.
TAXAS DE SUCESSO
Quanto à taxa de sucesso dos tratamentos de baixa complexidade, ela está muito relacionada com a causa da infertilidade, mas é inferior à das técnicas de alta complexidade.
Em pacientes anovulatórias, temos uma taxa de ovulação de 70% a 80% com estimulação ovariana e, quando esta é a única causa de infertilidade, a taxa de gravidez com coito programado chega até a 20-25% por ciclo, com uma taxa de gravidez cumulativa em seis meses de até 60-75% nestes casos. Após este tempo, o prognóstico é ruim. Em outros casos, as chances com coito programado são baixas.
Na inseminação intrauterina em pacientes abaixo de 30 anos, a taxa de gravidez é de 15% a 20%, mas acima de 37 anos cai para 6,2%. Quando levamos em consideração a causa, tem melhores resultados quando ela é ovulatória, por fator masculino leve ou sem causa aparente. Alterações tubárias e endometriose têm chances reduzidas.
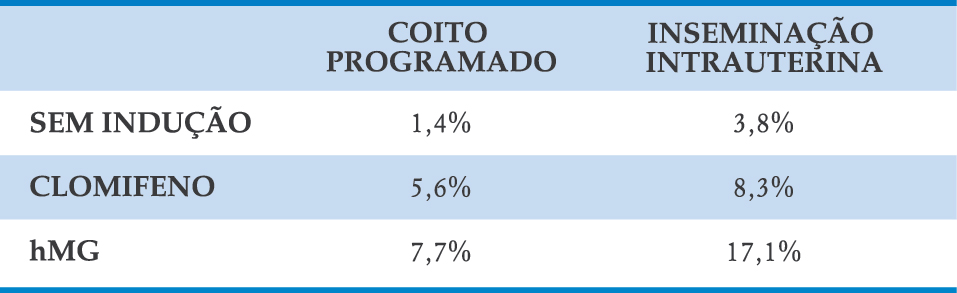
Nas pacientes com infertilidade sem causa aparente, a inseminação tem melhores resultados que o coito programado quando associada à estimulação ovariana. E o uso de gonadotrofinas tem resultados melhores que indutores orais (Quadro 6-7).
A maioria das gestações acontece nos primeiros quatro meses de tratamento. Nos casos em que o casal não engravida após seis meses de tratamento, outras técnicas de reprodução assistida devem ser conside¬radas, sempre individualizando o caso, levando-se em consideração a idade da paciente, um dos principais fatores prognósticos de sucesso dos tratamentos, o tempo de infertilidade e a causa.
QUADRO 6-7. TAXAS DE GRAVIDEZ/CICLO COM BAIXA COMPLEXIDADE EM PACIENTES COM INFERTILIDADE SEM CAUSA APARENTE