O primeiro bebê de fertilização in vitro (FIV), que recebeu o nome de Louise Brown, nasceu em 25 de julho de 1978 às 23h47 com 2,608 kg no Oldham General Hospital, em Oldham, Inglaterra, através de uma cesariana. Isso só foi possível depois de pesquisas realizadas desde 1966 pelo Dr. Patrick Steptoe, ginecologista do Hospital Geralde Oldham, e pelo Dr. Robert Edwards, um fisiologista da Universidade de Cambridge.
A FIV é a mais avançada das técnicas de reprodução assistida e a que produz as melhores taxas de sucesso, quando comparada às técnicas de baixa e média complexidade, como o coito programado e a inseminação intrauterina.
Para se realizar este procedimento, a mulher deve receber diferentes tipos de medicamentos para estimulação ovariana, geralmente com maiores doses do que na baixa e média complexidade, para se obter um maior número de oócitos recrutados. Os folículos também têm seu crescimento acompanhado por dosagens hormonais e pela ultrassonografia até que atinjam um diâmetro aproximado de 18 mm, e o endométrio, uma espessura superior a 7 mm.
Quando isso ocorre, a paciente recebe uma última medicação (hCG), que termina o amadurecimento dos óvulos, que são aspirados (ou coletados) ao redor de 35 horas depois, por meio de uma agulha conectada ao transdutor do ultrassom transvaginal. Em seguida, os óvulos são encaminhados ao laboratório que está acoplado à sala de coleta e submetidos ao processo de fertilização, que poderá ser pela FIV clássica (quando se coloca os espermatozoides em contato com os óvulos e a fecundação ocorre naturalmente) ou pela ICSI (Intracytoplasmic Sperm Injection ou Injeção Intracitoplasmática de Espermatozoide), que consiste na injeção de um espermatozoide dentro do óvulo. Os embriões são desenvolvidos e acompanhados no laboratório, sendo então transferidos ao útero. A chance de sucesso desta técnica pode chegar a até 60% em condições favoráveis e em pacientes com menos de 35 anos.
Índice
ToggleAs indicações clássicas
- mulheres com alterações peritoneais (aderências);
- obstrução tubária;
- Infertilidade Sem Causa Aparente (ISCA), ou infertilidade inexplicável;
- endometriose;
- falhas repetidas em tratamentos anteriores menos complexos;
- idade avançada;
- fator masculino (contagem baixa, alteração grave em morfologia ou motilidade dos espermatozoides);
- situações especiais, como ansiedade exagerada do casal, exaustão da relação afetiva dos dois em função da busca de um bebê, o casal morar em cidades distantes de Centros de Reprodução Humana, um dos membros do casal viajar muito e ter dificuldade de estar presente para ter relações no dia fértil, e outras.
Quais as condições mínimas necessárias?
- cavidade uterina normal;
- ovários funcionantes;
- número mínimo de espermatozoides;
- fazer a pesquisa da fertilidade (exames).
Quais os exames complementares mínimos e necessários para se realizar o procedimento?
- vídeohisteroscopia ou histerossalpingografia para avaliação da cavidade endometrial;
- ultrassom transvaginal: anatomia e reserva ovariana;
- exames gerais: doenças infecciosas e alterações hormonais;
- espermograma e exames gerais do homem.
Qual a característica do ovário? Atenção aos seguintes itens:
- idade da mulher;
- tamanho do ovário e o número de folículos antrais – baixa respondedora e SOP;
- reserva ovariana: FSH, LH, estradiol e hormônio antimulleriano (AMH);
- histórico de tratamentos anteriores: quais medicações, dose e como foi a resposta
Recursos mínimos para realizar um ciclo de FIV:
- ultrassom endovaginal;
- parceria com laboratório de análises clínicas que dê resultados rápidos;
- parceria com um profissional experiente ou Centro de Reprodução Humana;
- conhecimentos básicos das medicações, dos esquemas e complicações da indução da ovulação;
- estar atualizado sobre o que há de novo nos tratamentos de reprodução assistida.
O que casais gostam de saber? Perguntas mais frequentes:
- Qual a chance de sucesso?
- Qual a chance de gêmeos?
- Quantos embriões são transferidos?
- Qual a chance de malformação?
- É possível escolher o sexo?
- O que fazer com os embriões excedentes?
- Qual o custo?
- Quais os potenciais riscos de complicações e efeitos colaterais?
- Qual a duração média do tratamento?
A Técnica
A técnica é relativamente complexa, e sua execução pode ser dividida em seis fases:
1ª Fase – Bloqueio hipofisário

Consiste no bloqueio da hipófise por meio de agonista ou antagonista do GnRH. Com esta conduta, é possível ter o controle da função ovariana, não havendo perigo de ocorrer um pico de LH e a consequente ovulação fora do momento previsto. Este bloqueio poderá ser realizado antes ou depois do início da estimulação ovariana.
O bloqueio pode ser pelo protocolo “longo”, que se inicia no 21º dia do ciclo anterior, ou pelo protocolo “curto” que começa após alguns dias do início da estimulação ovariana (Quadro 7-1). Com a introdução do uso de agonistas/antagonistas ao ciclo de FIV, reduziu-se a luteinização prematura de 20% para menos de 2%.
QUADRO 7-1. TIPOS DE BLOQUEIO HIPOFISÁRIO PARA CICLOS DE FERTILIZAÇÃO IN VITRO

2ª Fase – Estímulo do crescimento e desenvolvimento dos folículos:
Existem vários esquemas de medicação para estimular o crescimento de um maior número de folículos que, pela maior quantidade, poderão aumentar as chances de gravidez. A estimulação ovariana se faz normalmente com uso de FSH recombinante ou FSH urinário. Pode-se também usar hMG, uma associação de FSH+LH urinário, ou adicionar LH recombinante. Pode-se ainda usar FSH de ação prolongada (detalhe de todos os medicamentos no Capítulo 4). Esta fase dura de oito a 12 dias e é acompanhada pelo ultrassom transvaginal e por dosagens hormonais. Quando os maiores folículos atingem 18 mm, para-se a estimulação hormonal e é simulado um pico de LH para completar a maturação final dos oócitos (reativar a meiose que estava parada em Profase I). Isto é feito com hCG recombinante ou urinário. Em situações especiais, em ciclos com antagonista, pode-se utilizar agonista do GnRH no lugar do hCG.
O objetivo da indução da ovulação é estimular o crescimento de alguns folículos para o posterior estágio de maturação. Os protocolos mais utilizados são:
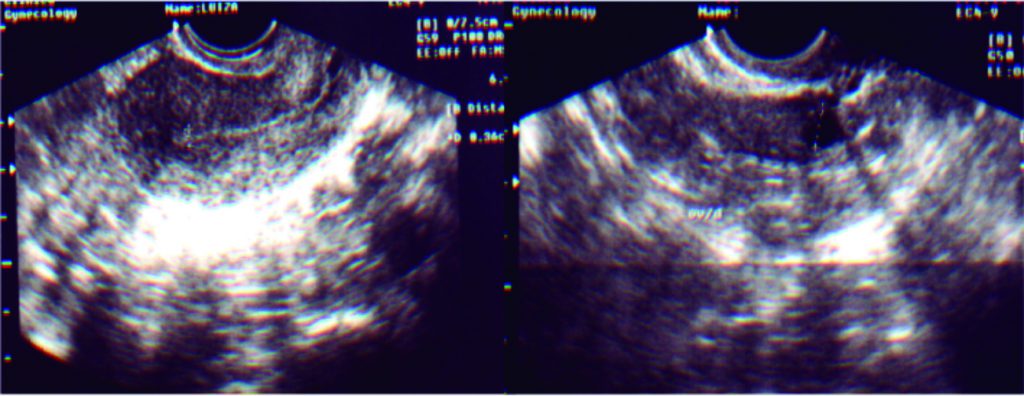
1- Protocolo longo: Down–Regulation da hipófise é obtido com agonistas do GnRH. O início das aplicações é no 21º dia do ciclo anterior à indução da ovulação. São aplicações diárias subcutâneas (Lupron) ou em dias alternados (Gonapeptyl daily), injeções únicas de depósito (Lupron depot, Lorelim, Zoladex ou similares) ou aplicações nasais (Synarel). São administradas durante 10-15 dias até o bloqueio total da hipófise, quando o estradiol atinge níveis extremamente baixos (< 50 pg/mL). A finalidade deste bloqueio é impedir o pico de LH, o que poderia provocar uma ovulação inesperada, antes do momento da captura dos óvulos. Após a menstruação, ao redor do 3º dia do ciclo menstrual, quando o endométrio tiver uma espessura fina, ao redor de 3 mm, e os ovários não tiverem folículos maiores que 10 mm, remanescentes do ciclo menstrual anterior, a estimulação ovariana é iniciada (Figura 7-1). Neste momento, a dose do agonista geralmente deverá ser reduzida pela metade. O bloqueio se manterá até o final da estimulação ovariana (Quadro 7-2).
FIGURA 7-1. ULTRASSOM NO 3º DIA DO CICLO APÓS BLOQUEIO COM AGONISTA
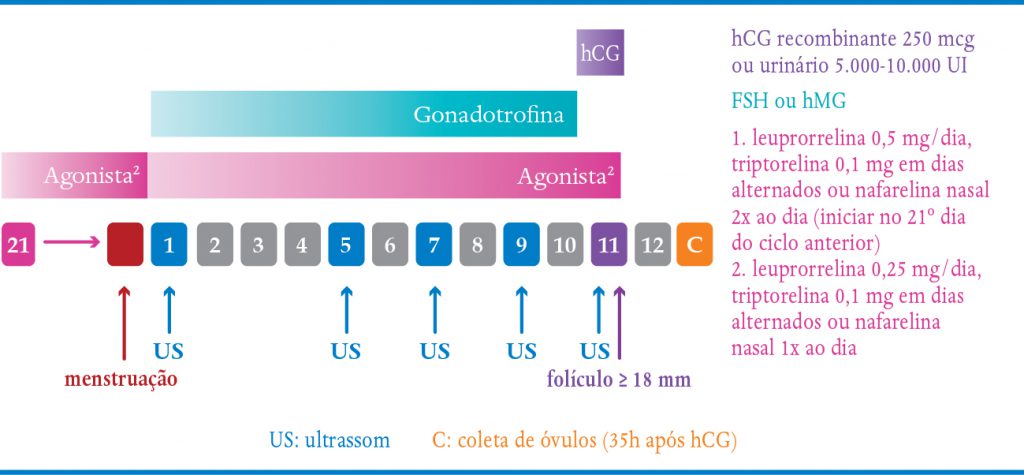
QUADRO 7-2. PROTOCOLO LONGO COM AGONISTA
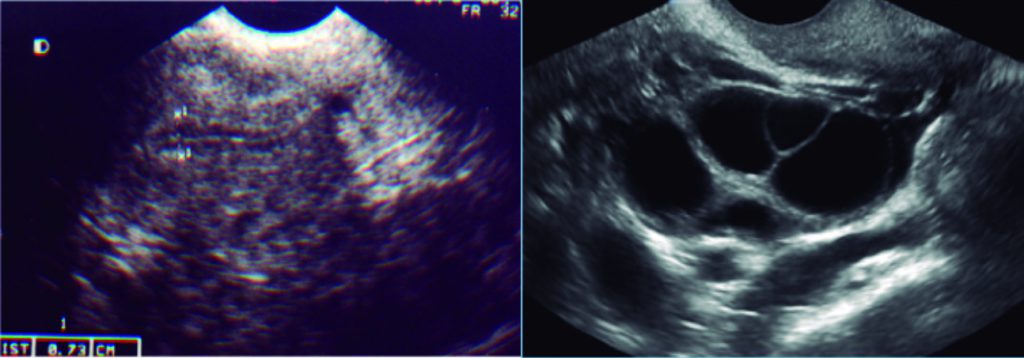
Um novo controle ultrassonográfico é repetido no 5º dia de estimulação para acompanhar o crescimento dos folículos e do endométrio (Figura 7-2). Deverão ser medidos todos os folículos pelo seu diâmetro médio. De acordo com o ultrassom, pode-se alterar a dose e o tipo de gonadotrofina utilizada.
FIGURA 7-2. CONTROLE ULTRASSONOGRÁFICO NO 5º DIA DA ESTIMULAÇÃO OVARIANA PARA CICLO DE FERTILIZAÇÃO IN VITRO
Segue-se então mantendo-se a estimulação e o bloqueio diariamente, com controle ultrassonográfico em dias alternados. Quando os maiores folículos atingem mais de 18 mm, uma ampola de hCG é aplicada. Neste dia, normalmente não se faz a dose da gonadotrofina, somente o bloqueio (Figura 7-3). A coleta dos óvulos é então agendada para 35 horas após o hCG. Dosagem de estradiol e progesterona podem ser úteis neste momento.
FIGURA 7-3. CONTROLE ULTRASSONOGRÁFICO NO 11º DIA DA ESTIMULAÇÃO OVARIANA PARA CICLO DE FERTILIZAÇÃO IN VITRO

2-Protocolo curto com antagonista: a supressão da hipófise é feita pelo antagonista do GnRH (Orgalutran ou Cetrotide). O antagonista tem a mesma função que o agonista do GnRH, mas tem a vantagem de causar um bloqueio hipofisário imediato, sem o efeito flare-up inicial, assim, pode ser administrado depois do início da estimulação, levando a paciente a receber menos picadas. Por isso, hoje em dia, tende a ser mais utilizado que o protocolo longo. Como no protocolo anterior, realiza-se um ultrassom entre 2º e 3º dia do ciclo, para avaliar ausência de cistos e endométrio fino.
Inicia-se então as gonadotrofinas, com controles ultrassonográficos também no 5º dia e então em dias alternados.
Existem várias propostas em relação ao momento ideal de iniciar o antagonista, que variam entre o 5º e o 6º dia da indução ou, para alguns, quando os folículos atingirem o diâmetro de 14 mm. Cada clínica tem a sua preferência, o IPGO tem preferido utilizar o protocolo flexível, ou seja, quando a dimensão do maior folículo atinge 14 mm (Quadro 7-3). Uma vez iniciando o antagonista, mantém-se até o dia do hCG, que tem critérios de realização idênticos ao protocolo longo.
A maior vantagem deste protocolo está nos casos de pacientes que têm risco de ter Síndrome de Hiperestimulação Ovariana. Nestes casos o hCG que finaliza a maturação folicular é trocado por uma dose única do agonista de GnRH, e com isso evitam-se as complicações desta Síndrome.
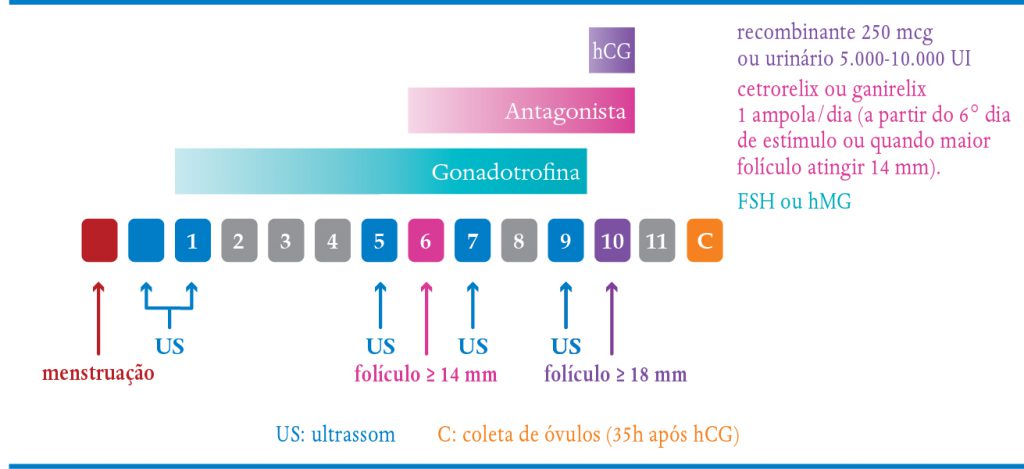
QUADRO 7-3. PROTOCOLO CURTO COM ANTAGONISTA
Protocolo com FSH de ação prolongada – Elonva (corifolitropina alfa): não há dúvidas de que uma reclamação frequente das mulheres que passam por um ciclo de FIV é o fato de precisarem tomar injeções diárias durante alguns dias. Embora este período normalmente não ultrapasse os dez dias, algumas pacientes chegam a desistir do tratamento por certo tempo e às vezes para sempre, por considerarem esta fase um sofrimento inesquecível.
Elonva é uma injeção única que vale por sete dias de aplicação de FSH, substituindo as aplicações diárias neste período (Quadro 7-4). É utilizada em mulheres submetidas a tratamentos de infertilidade que necessitam de estimulação ovariana para o desenvolvimento de mais que um óvulo maduro de cada vez. É administrada em dose única por injeção subcutânea. As mulheres que pesam 60 kg ou menos devem receber uma dose de 100 microgramas, ao passo que as mulheres que pesam mais de 60 kg devem receber uma dose de 150 microgramas. A própria paciente ou o seu parceiro podem aplicar a injeção no caso de terem recebido as instruções adequadas.
QUADRO 7-4. BIOATIVIDADE DO FSH COM ELONVA E COM INJEÇÕES DIÁRIAS DE FSH RECOMBINANTE (rFSH)
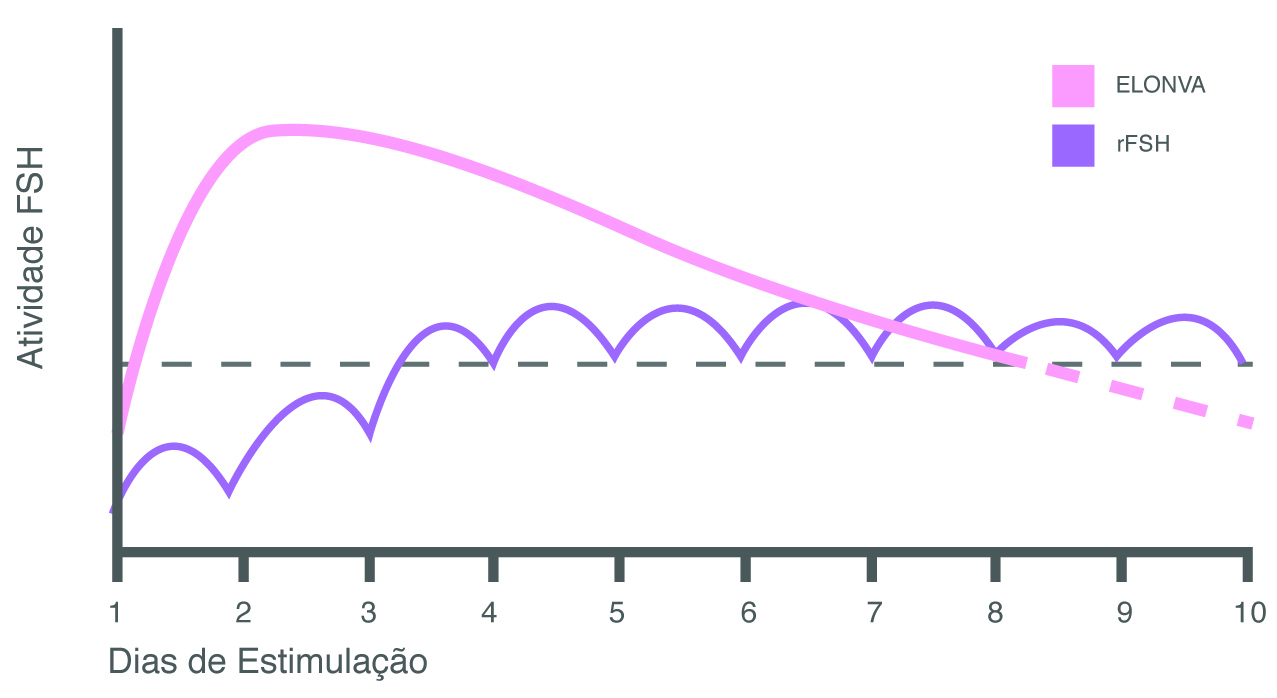
Cinco dias após a injeção do Elonva, dependendo da resposta dos ovários, inicia-se o tratamento com um antagonista da GnRH, que impede uma liberação prematura dos óvulos pelos ovários. Sete dias após a injeção do Elonva, no caso de ser necessária uma estimulação ovariana adicional, podem ser administradas injeções diárias de gonadotrofinas (FSH ou FSH+LH), até o momento de se realizar o hCG. Elonva (corifolitropina alfa) tem ação semelhante a outros medicamentos que contêm FSH também utilizados para estimular os ovários nos tratamentos de fertilidade, mas tem a diferença de possuir uma ação prolongada no organismo. Em resultado disto, pode ser administrada uma dose única, substituindo desta forma sete injeções diárias necessárias para estes outros (Quadro 7-5).
QUADRO 7-5. PROTOCOLO DE ESTIMULAÇÃO OVARIANA COM ELONVA EM CICLO COM ANTAGONISTA
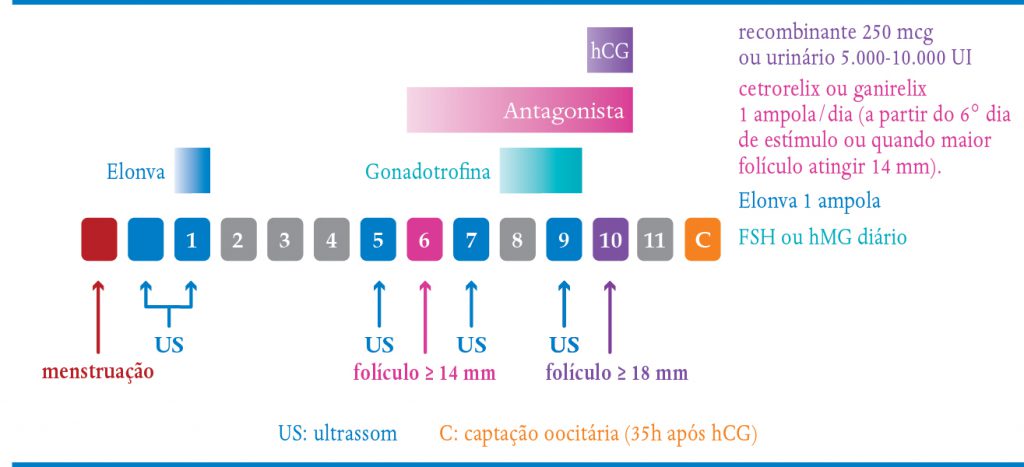
3ª Fase – Coleta dos óvulos
Os folículos são aspirados através de uma agulha acoplada ao transdutor transvaginal e conectada a um sistema de aspiração, em um ambiente cirúrgico (Figura 7-4), 35h após a administração do hCG. Pode ser realizada com anestesia local mas, geralmente, opta-se por uma sedação profunda (Propofol). Este processo é indolor e dura alguns minutos. O conteúdo folicular é diretamente encaminhado para avaliação pelo embriologista. Neste dia, é também realizada a coleta do sêmen do marido.
FIGURA 7-4. COLETA DE ÓVULO

Equipamentos Necessários para Coleta de Óvulos:
• sala especial acoplada ao laboratório;
• US transvaginal;
• agulha acoplada ao transdutor;
• sistema de sucção;
• equipamento mínimo de anestesia (ECG, Oxímetro, Pressão não invasiva, Propofol).
4ª Fase – Fertilização dos óvulos
No laboratório, após a aspiração, os óvulos são separados, cultivados e classificados quanto à sua maturidade. Posteriormente, a fertilização poderá ocorrer de quatro maneiras:
FIV clássica: os óvulos são colocados em uma incubadora no laboratório, junto dos espermatozoides, em condições ambientais semelhantes às encontradas na trompa uterina – local em que normalmente ocorre a fecundação (Figura 7-5).
ICSI (Intracitoplasmatic Sperm Injection ou Injeção Intracitoplasmática de Espermatozoide): quando a quantidade de espermatozoides for pequena, os óvulos são fertilizados através da micromanipulação dos gametas, injetando-se um espermatozoide em cada óvulo. A seleção dos espermatozoides para a ICSI é feita pela avaliação visual da motilidade e morfologia (Figura 7-5).
FIGURA 7-5. FERTILIZAÇÃO IN VITRO PELA FORMA CLÁSSICA E POR ICSI

ICSI Magnificado, Super-ICSI ou IMSI (Intracytoplasmic Morfologically Select Sperm Injection): é uma técnica que identifica com precisão os espermatozoides com maior capacidade de fertilização, usada quando houver alterações no seu formato (morfologia alterada), presença de vacúolos e fragmentação do DNA espermático. Utiliza um sistema ótico que apresenta objetivas de maior poder de ampliação eletrônica das imagens, podendo observar os espermatozoides em detalhes, detectar seus defeitos e selecionar os melhores, pois são aumentados em até 12.500 vezes. Identifica em tempo real e com precisão os espermatozoides com maior capacidade de fertilização avaliando um conjunto de alterações que são denominadas pela sigla em inglês MSOME (Motile Sperm Organellar Morphology Examination). Espermatozoides com estas alterações podem formar embriões de má qualidade e o consequente insucesso da FIV. O IMSI ou “Super ICSI” pode ser indica¬do principalmente para casais cujo homem tem alterações importantes da morfologia dos espermatozoides, insucesso em tratamentos anteriores de FIV, altas taxas de fragmentação do DNA dos espermatozoides e abortos repetidos. Com esta nova técnica espera-se que a taxa de gravidez, que nestes casos pode estar abaixo do esperado, possa alcançar valores próximos a 60%, dependendo da idade da mulher.
PICSI (Physiological Intracytoplasmatic Sperm Injection): a seleção ocorre entre os espermatozoides que se ligam (in vitro) a um “componente especial”, também presente na camada externa do óvulo (uma placa de ácido hialurônico). Em pesquisas recentes foi demonstrado que os espermatozoides selecionados pela PICSI (que se unem a esta placa) são maduros, possuem menos danos ao DNA e são sujeitos a menos aneu¬ploidias (doenças genéticas) que os espermatozoides selecionados pela ICSI convencional. É indicado nos casos de fragmentação do DNA dos espermatozoides acima de 30%.
Em qualquer uma dessas técnicas, 18 horas após a coleta dos óvulos é confirmada a fertilização e, assim, passam a se chamar pré-embriões, cujo crescimento é acompanhado até o momento da transferência ou vitrificação. Nesta fase poderá ser realizada a biópsia embrionária – PGD (Pré-Implantation Genetic Diagnosis) ou DPI (Diagnóstico Pré-Implantacional) para pesquisa de aneuploidias ou doenças genéticas.
Clique abaixo e veja os vídeos:
ICSI
5ª Fase – Transferência do(s) embrião(ões) para o útero
Dois a cinco dias após a fertilização, os embriões são transferidos para o útero. Neste dia, serão conhecidos os de melhor qualidade, e assim o médico especialista, o embriologista e o casal decidirão juntos quantos deles serão transferidos, número este que pode variar de um a quatro e que dependerá das regras da ética, da idade da mulher e da qualidade dos embriões.
Avaliação da qualidade dos embriões e escolha do dia da transferência (3º ou 5º dia?): no dia seguinte à fertilização, que ocorre horas após a aspiração dos óvulos, os embriões são analisados para verificar qual a porcentagem dos óvulos maduros que foram fertilizados. Na maioria das vezes, mesmo nos casos de ICSI, uma parte destes óvulos não se fertiliza. Já neste momento pode ser feita uma análise inicial microscópica e prognóstica da qualidade destes embriões e quais são os que têm maior chance de sobreviver e alcançar um estágio mais avançado de divisão celular. No 3º dia, estes embriões são mais uma vez estudados para que se faça uma nova classificação dos melhores. Esta classificação é baseada na “MORFOLOGIA”. Na morfologia do embrião, dois itens são analisados: o número de células (deverá ser de 6 a 8) e o índice de fragmentação (Figura 7-6). Quanto menor o grau de fragmentação e número adequado de células, teoricamente, melhor será este embrião e maior será a chance de implantação.
Existem ainda outras formas não invasivas de avaliar o embrião, entre elas:
- taxa de respiração dos embriões (consumo de O2);
- spindle view;
- expressão gênica;
- meios de cultura individualizados;
- metabolomics;
- time lapse (embrioscópio).
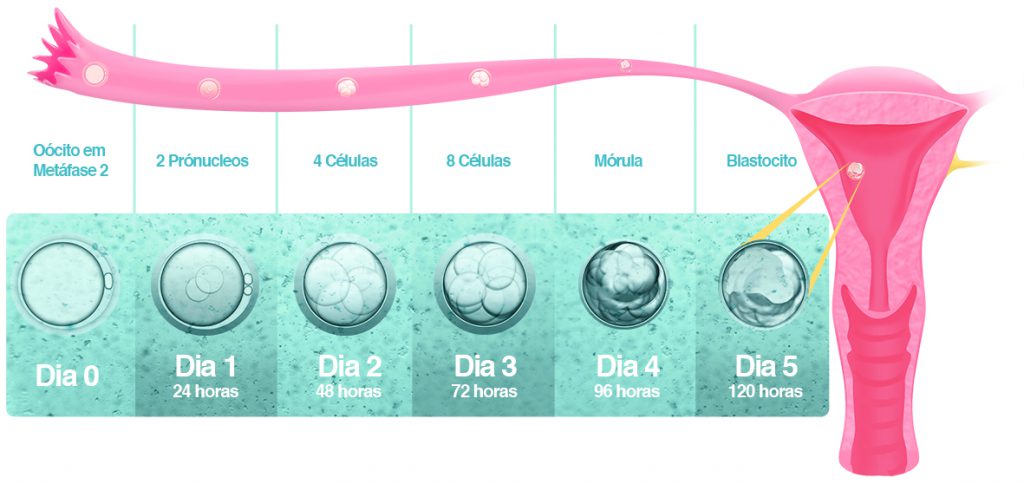
Normalmente, por vias naturais, o embrião chega à cavidade uterina com cinco ou seis dias de vida, em um estágio chamado BLASTOCISTO. Assim, parece claro que, quando transferimos para a mulher embriões neste estágio (ou seja, 5 ou 6 dias após a coleta dos óvulos), a chance de gravidez pode ser maior. Entretanto, nem sempre conseguimos que o embrião chegue a este estágio no laboratório e, além do mais, exis¬te uma perda considerável no número de embriões durante estes cinco dias de desenvolvimento
FIGURA 7-6. AVALIAÇÃO MORFOLÓGICA DO EMBRIÃO ATÉ O 5º DIA DE DESENVOLVIMENTO


Clique e veja o vídeo abaixo:
Transferência de embriões
Veja a resolução 1957 do CFM:
Comentário importantíssimo:
Ao classificarmos um embrião de melhor ou pior, não estamos concluindo que as crianças nascidas destes embriões terão saúde diferente uma das outras. Significa simplesmente, que, ao implantar os embriões que passaram pelo período de divisão celular inicial com facilidade, a chance de gerar uma gravidez deve ser estatisticamente maior.
O embrião morfologicamente “mais feio” (menos células e mais fragmentado) poderá ter uma chance menor de implantação, mas gerar uma criança 100% saudável.
Se no 3º dia após a fertilização tivermos um número excessivo de embriões (superior a 4), uma boa conduta é aguardarmos que estes embriões atinjam a fase de BLASTOCISTOS para que os melhores passem por mais esta prova de seleção. Assim, no 5º ou 6º dia, os embriões que atingirem esta fase serão os que terão maior chance de implantação.
E, mais uma vez, a decisão do dia da transferência será feita após a coleta dos óvulos e a avaliação inicial dos embriões. Dependerá de algumas variáveis importantes, por exemplo, idade da paciente, número de tentativas anteriores, número de óvulos coletados/maduros e, ainda, número e qualidade dos embriões obtidos.
Número de embriões transferidos: o Conselho Federal de Medicina (CFM), desde a resolução CFM nº 1.957/2010 (Normas Éticas para a Utilização das Técnicas de Reprodução Assistida), definiu:
“O número máximo de oócitos e embriões a serem transferidos para a receptora não pode ser superior a quatro. Em relação ao número de embriões a serem transferidos, são feitas as seguintes determinações:
a) mulheres com até 35 anos: até dois embriões;
b) mulheres entre 36 e 39 anos: até três embriões;
c) mulheres com 40 anos ou mais: até quatro embriões.”
Essa norma é importante para diminuir o número de gestações múltiplas, fixando um número máximo de embriões de acordo com a idade. Como quanto maior a idade da mulher, menor a chance de implantação, podemos colocar mais embriões em mulheres com idades mais avançadas. Entretanto, não leva em conta a qualidade do embrião e se o embrião está em D3 ou blastocisto. Como blastocistos apresentam maior taxa de implantação que embriões em D3, tendemos a colocar um menor número de embriões quando estão nesta fase (Quadro 7-6).
QUADRO 7-6. ESQUEMA DO NÚMERO DE EMBRIÕES TRANSFERIDOS

Importante:
1. Embriões excedentes não são descartados de imediato. Caso seja fer-tilizado um número maior de embriões que o esperado, o excedente poderá ser congelado (vitrificado) para utilização posterior. Se o casal não desejar ter mais filhos, poderá doá-los para outro casal, para a pesquisa científica ou, segundo a CFM nº 2013/13 do Conselho Federal de Medicina (CFM), poderão ser descartados após cinco anos.
2. Os casais que em nenhuma hipótese concordarem com o congela¬mento dos embriões poderão ter um número limitado de óvulos fertilizados, impedindo assim o excesso e a necessidade do congelamento (vitrificação).
Técnica de transferência de embriões:
A transferência é indolor, realizada sob a visão do ultrassom, com cateter flexível, geralmente sem anestesia, através da vagina. O(s) embrião(ões) deve(m) ser colocado(s) de 1,5 cm a 2 cm abaixo do fundo uterino. Este procedimento é indolor e semelhante ao desconforto do exame ginecológico. A passagem do cateter deve ser um movimento delicado, pois as chances de gravidez têm muita ligação com este momento. Trata-se de um procedimento simples, mas que exige tranquilidade, um bom relaxamento da paciente e experiência do profissional (Figura 7-7). Após essa etapa, a paciente deverá ficar deitada por cerca de 20 a 30 minutos, retornando posteriormente para casa com atividades físicas limitadas e orientada com as devidas medicações.
FIGURA 7-7. TRANSFERÊNCIA DE EMBRIÕES
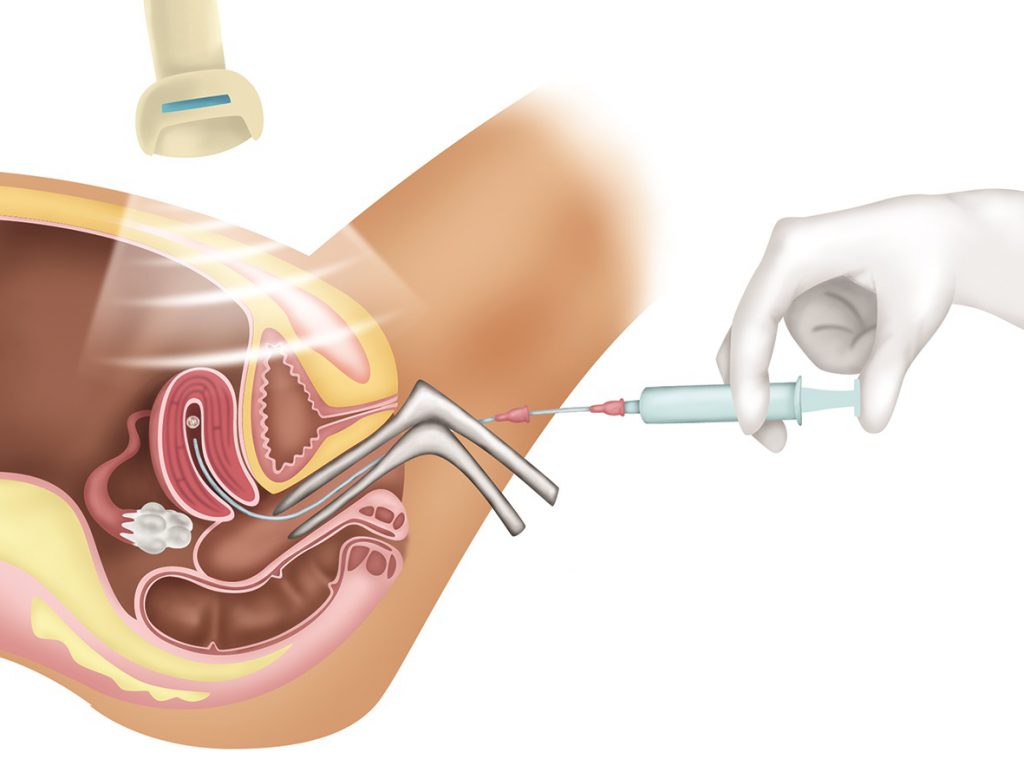
Recomendações para realizar uma boa transferência embrionária:
- Histeroscopia prévia. Dá a oportunidade de se avaliar as imperfeições do colo uterino, suas irregularidades e eventuais estreitamentos (estenoses). Caso sejam observadas estas alterações, o médico especialista poderá tomar providências antes do início do procedimento. Na impossibilidade, uma opção é realizar um teste com cateter através do orifício interno do colo antes da transferência.
- Histerometria prévia (medida do útero) durante o controle da ovulação. Esta medida ajudará o especialista a dar a curvatura ideal no cateter e posicioná-lo da maneira adequada, principalmente nos úteros retrovertidos, e permitirá a colocação dos embriões no melhor local para a implantação. Evitará também que o cateter toque o fundo uterino e cause sangramentos indesejáveis.
- Ultrassom transabdominal com a bexiga parcialmente cheia durante a transferência. Médicos experientes nem sempre precisam deste acompanhamento, embora mostre melhores resultados, além de permitir que a paciente tenha visualização de que os embriões foram colocados no lugar.
- Lavagem do colo com meio de cultura para remover o excesso de muco com cotonete ou aspiração com seringa.
- Cateter de Sidney, com 30 microlitros de meio de cultura, contendo embriões nos últimos 10 microlitros do fluido e a coluna de fluido contínuo com a seringa.
- Inserção lenta do cateter guiado por ultrassom, para evitar que toque no fundo do útero.
- Depositar o embrião na área central do endométrio.
- Injetar os embriões lentamente a 1,5-2 cm do fundo, confirmado por ultrassom.
- Retirar o cateter lentamente.
- Inspeção do cateter pelo embriologista para verificar sangue, muco e embriões retidos. Caso haja embriões retidos no cateter, repetir o procedimento.
6ª Fase – Suporte hormonal:
No dia seguinte à coleta de óvulos, inicia-se o suporte hormonal com progesterona. As doses são ajustáveis de acordo com a necessidade da paciente. São utilizadas uma das seguintes opções:
- progesterona injetável (Progesterone): 50 a 100 mg/dia – intramuscular;
- micronizada (Utrogestan/Evocanil): 600 a 1200 mg/dia – via vaginal;
- gel (Crinone 8%): 1 a 2x/dia, via vaginal.
Em algumas situações pode ser adicionado o Duphaston (didrogesterona 10 mg 12/12h via oral). Quando a paciente tiver poucos óvulos, o suporte da fase lútea poderá ser feito com três doses de hCG 1.500U SC a cada três dias. Não se deve utilizar hCG para suporte na fase lútea se o número de óvulos for maior pelo risco de Síndrome de Hiperetimulação Ovariana.
Durante a fase lútea, podem ser realizados exames de sangue que comprovam o equilíbrio hormonal (Estradiol > 200 pg/mL e progesterona > 20 ng/mL). Caso haja necessidade, as doses da progesterona poderão ser modificadas e/ou introduzido reposição de estradiol.
O teste de gravidez é realizado 11 dias após a transferência dos embriões.
RESUMO EXPLICATIVO DO ACOMPANHAMENTO MÉDICO EM FIV
Protocolo longo:
- Ácido fólico + vitamina C e vitamina E.
- Iniciar agonista no 21º dia do ciclo anterior.
- Ultrassom transvaginal no 2º-3º dia da menstruação para verificar a inexistência de cistos remanescentes do ciclo anterior. Caso haja folículo > 10mm, a dosagem do estradiol plasmático pode ajudar bastante. Se < 50 pg/mL, pode iniciar estímulo.
- Iniciar estimulação ovariana com gonadotrofinas ao redor do 3º dia da menstruação (dose variável). Diminuir dose do agonista.
- Monitorização do crescimento dos folículos e da espessura do endométrio, para ajuste da dose: 5º dia de estímulo e, então, dias alternados.
- Quando pelo menos dois folículos > 18 mm, administrar hCG. Neste dia, não é necessário administrar a gonadotrofina, somente o agonista.
- Coleta dos óvulos 35 h após hCG.
- Suporte fase lútea (dia seguinte da coleta).
- Transferência embrionária (3º ou 5º dia após a coleta).
- Beta-hCG 11 dias após a transferência.
Protocolo curto:
- Ácido fólico + vitamina C e vitamina E.
- Ultrassom transvaginal no 2º-3º dia da menstruação para verificar a inexistência de cistos remanescentes do ciclo anterior. Caso haja folículo > 10mm, a dosagem do estradiol plasmático pode ajudar bastante. Se < 50 pg/mL, pode iniciar.
- Iniciar estimulação ovariana com gonadotrofinas ao redor do 3º dia da menstruação (dose variável).
- Monitorização do crescimento dos folículos e da espessura do endométrio, para ajuste da dose: 5º dia e então em dias alternados.
- Iniciar antagonista quando maior folículo atingir 14 mm.
- Quando pelo menos dois folículos > 18 mm, administrar hCG. Neste dia, não é necessário administrar a gonadotrofina, somente o antagonista.
- Coleta dos óvulos 35 h após hCG.
- Suporte fase lútea (dia seguinte da coleta).
- Transferência embrionária (3º ou 5º dia após a coleta).
- Beta-hCG 11 dias após a transferência.
TAXAS DE SUCESSO
• O sucesso da FIV vai depender de vários fatores:
• idade da mulher;
• qualidade dos óvulos e espermatozoides;
• qualidade dos embriões;
• qualidade endometrial;
• transferência do embriões.
Entretanto, mesmo quando todos os parâmetros são favoráveis, ainda há chance de insucesso. A idade da mulher é o maior preditor de sucesso da FIV, caindo progressivamente com o avançar da idade. Enquanto mulheres abaixo dos 35 anos têm taxa de gravidez de mais de 50% em ciclos de FIV, essa taxa cai pra menos de 20% nas maiores de 40 anos (Quadro 7-7). Portanto, cabe ao ginecologista alertar a mulher acima dos 35 anos que não pode esperar muito, pois mesmo com tratamento suas chances caem bastante.
QUADRO 7-7. TAXA DE GRAVIDEZ POR TRANSFERÊNCIA EMBRIONÁRIA DE ACORDO COM A IDADE MATERNA

Conheça o diagnóstico pré implantacional – PGD / DPI
Outras considerações
Congelamento de embriões (vitrificação)
No início de um tratamento de FIV, uma questão bastante importante para médicos e casais diz respeito ao número de óvulos que potencialmente serão produzidos durante o ciclo. Este dado inicialmente parece ser de pouca relevância, mas torna-se importante, pois o número de óvu¬los a serem produzidos está diretamente relacionado ao número de embriões que serão obtidos. Um número ideal de embriões oferece melhores condições para cultivos mais longos, como cultura de blastocistos.
No entanto, a obtenção de números altos de óvulos pode gerar uma grande quantidade de embriões excedentes ao ciclo realizado. Segundo o Conselho Federal de Medicina, atualmente os embriões excedentes aos ciclos de FIV podem ter quatro destinos: congelamento (vitrificação), doação a outro casal, doação à pesquisa científica e, por último, o descarte, após cinco anos de congelamento e se for do interesse do casal (Resolução CFM 2013/13).
O congelamento de embriões possui uma longa história dentro da medicina reprodutiva, com nascimento na metade da década de 1980, sendo, hoje, comprovadamente um procedimento já bastante dissemi¬nado nos centros de reprodução humana espalhados pelo mundo. Neste campo, existe uma variedade de leis que geralmente mudam de acordo com o país. Mas, de um modo geral, o congelamento de embriões é aceito pela maioria.
Ele não deve ser o objetivo do tratamento, mas possibilita que casais que produzam números altos de óvulos e, consequentemente, embriões, possam ter mais uma chance para obter a sua tão desejada gestação sem a necessidade de um novo estímulo ovariano. Do mesmo modo, casais que conseguiram ter sucesso na primeira tentativa e congelaram alguns embriões excedentes podem voltar depois de alguns anos e utilizar estes mesmos embriões para uma segunda tentativa. Os embriões a serem congelados (vitrificados) são estocados a -196 ºC em nitrogênio líquido. O tempo de permanência em nitrogênio líquido parece afetar pouco a viabilidade embrionária, já existindo casos de gestações após um período de oito anos de congelamento. A perda de viabilidade durante o armazenamento pela técnica de vitrificação é praticamente inexistente, contudo, ainda existem dúvidas quanto ao período máximo que os embriões poderiam aguentar.
Mesmo que ainda existam interrogações com relação aos processos de congelamento, o número de procedimentos realizados até agora e o índice de sucesso por tentativa mostram que este é um procedimento que oferece bons índices de sucesso e deve ser utilizado quando for necessário, ou seja, naqueles casais que produzem um alto número de embriões.
Algumas vezes, opta-se pro congelar todos os embriões para transferi-los em um ciclo natural ou com preparo endometrial. Isso ocorre por exemplo quando se usa protocolos alternativos com associação de citrato de clomifeno, há elevação dos níveis de progesterona antes do hCG (Capítulo 11), risco de Síndrome de Hiperestimulação Ovariana (Capítulo 10) ou níveis muito elevados de estradiol durante a estimulação.
Armazenamento de embriões
Quando a mulher produz poucos óvulos por ciclo, uma conduta possível é o acúmulo de embriões por meio de várias coletas. Estes casais poderiam fazer vários ciclos com números baixos de embriões e congelá-los. Depois de alguns meses, este “estoque” de embriões seria utilizado de uma só vez, para maximizar suas chances. Este procedimento é muito realizado com os ciclos espontâneos, ou seja, quando só ocorre a produção de um óvulo, ou naquelas mulheres em que a produção de óvulos é muito baixa.
As induções da ovulação podem ser repetidas, isto é, os óvulos são coletados em duas ou três induções diferentes, em meses seguidos ou não, fertilizados, congelados (vitrificados) e transferidos, de uma só vez, em um ciclo seguinte. Esta possibilidade é interessante por reduzir as pressões emocionais, somadas nas várias tentativas que serão reduzidas a uma única transferência.
COMPLICAÇÕES
As complicações da FIV são incomuns e em geral não são graves, mas em uma pequena parcela de casos a situação pode se complicar e levar até a óbito. Essas complicações podem ser divididas em quatro grupos:
1-Complicações agudas decorrentes da estimulação ovariana
O ovário pode responder demais e levar à Síndrome de Hiperestimulação Ovariana (SHO). Casos leves têm frequência de até 20%, moderados de 3-6% e, em sua forma mais severa, ocorre entre 0,5 a 2% dos ciclos de estimulação ovariana. Atualmente, a SHO tem diminuído de frequência devido ao uso de novos protocolos.
2-Complicações decorrentes da coleta de óvulos:
• Lesão da artéria ilíaca: é muito rara. Pode levar à laparotomia de urgência, com grande chance de complicações sérias.
• Sangramento ovariano após punção: também infrequente (0,5% dos casos), mas pode necessitar de internação para observação e até abordagem cirúrgica para cauterização.
• Infecção pós-punção: descrita em cerca de 0,3% dos casos, necessitan¬do em casos mais graves de tratamento antibiótico e até cirúrgico.
3-Complicações obstétricas:
• Gravidez múltipla: chega a até 20% das gravidezes de FIV.
• Pré-eclâmpsia, prematuridade, descolamento de placenta, restrição de crescimento fetal e baixo peso ao nascer: bebês de FIV/ICSI têm até duas vezes mais risco de restrição de crescimento, baixo peso ao nascer e parto prematuro. Além disso, há maior risco da gestante desenvolver pré-eclâmpsia e ter descolamento de placenta. Entretanto, essas complicações só ocorrem em ciclos de FIV com embriões a fresco, não se vendo em ciclos com embriões congelados. Isso se deve ao fato dos níveis elevados de estradiol num ciclo de FIV alterarem a placentação, o que leva a essas complicações, sendo uma boa opção optar pelo congelamento dos embriões quando os níveis de estradiol se elevam muito.
• Malformações fetais: existe uma maior incidência de malformações fetais em fetos concebidos in vitro em relação aos de gestações espontâneas (risco relativo: 1.32; intervalo de confiança: 1.24-1.42).
4- Aumento do risco de câncer?
Apesar de já ter sido levantada essa possibilidade, as últimas meta-análises não demonstraram aumento de risco de câncer de mama, colo, endométrio ou ovário em pacientes submetidas a ciclos de FIV.
Este texto foi extraído do e-book “Manual Prático de Reprodução Assistida para a Enfermagem”.
Faça o download gratuitamente do e-book completo clicando no botão abaixo:
