Com os cuidados corretos, esta possibilidade ficou muito rara.
Após esta leitura, leia também:
Por que a fertilização in vitro pode falhar
Fertilização in vitro em mulheres maduras
Tratamentos que podem melhorar a fertilidade da mulher
“Amazenamento” de embriões
Intralipid®
Menopausa precoce falência ovariana
SOP
Qual o custo?
A Síndrome da Hiperestimulação Ovariana (SHO) é uma complicação decorrente do estímulo ovariano com indutores de ovulação, podendo levar a quadros graves e, em casos extremos, até à morte. Geralmente é decorrente de uma resposta exacerbada dos ovários ao estímulo hormonal e resulta em um número grande de oócitos. Embora nestas condições este número costume ser superior a vinte, algumas vezes um número menor pode trazer a mesma consequência. É a complicação mais comum neste tipo de tratamento, principalmente quando a estimulação é realizada por médicos ainda com pouca experiência. Por isso, recomendamos que o ginecologista geral tenha sempre por perto o apoio de um profissional que tenha experiência neste tipo de intercorrência.
Casos leves têm frequência de até 20%, moderados, de 3-6%, e, em sua forma mais severa, ocorrem entre 0,5% e 2% dos ciclos de estimulação ovariana. Apesar de ser geralmente autolimitada, especialmente na ausência de gravidez, é uma das mais sérias complicações da Reprodução Assistida (RA) e representa um risco à vida se não identificada e manejada adequadamente. A mortalidade é baixa – cerca de três óbitos a cada 100 mil ciclos. Entretanto, se considerarmos que cerca de 1 milhão e meio de ciclos de RA são realizados no mundo por ano, estima-se que quase 50 mulheres morrem ao ano em decorrência dessa complicação. Além disso, cerca de 10% dos ciclos são cancelados pelo risco de SHO, representando frustração para a paciente, além de desperdício financeiro e de tempo.
FISIOPATOLOGIA
Sua fisiopatologia está relacionada ao aumento da permeabilidade vascular, com passagem massiva de fluidos do espaço intravascular para o terceiro espaço com acúmulo de líquidos neste (ascite, derrame pleural, pericárdico etc.), associada a profunda depleção do volume intravascular e hemoconcentração.
Acredita-se que, com a ação do hCG na granulosa, ocorra a produção e liberação de substâncias vasoativas, entre elas o VEGF (vascular endothelial growth factor, ou fator de crescimento vascular endotelial). Este tem ação em receptores endoteliais, levando ao aumento da permeabilidade vascular. Assim, quando se tem muitos folículos, a produção desse mediador estará muito aumentada e, portanto, ocorrerá um aumento importante da permeabilidade vascular, levando ao extravasamento de líquido do espaço intravascular para o extravascular.
Há duas formas clínicas principais da SHO: precoce e tardia, dependendo do momento de início. A SHO precoce é induzida pelo hCG exógeno administrado para a maturação oocitária final, ocorrendo geralmente dentro de 3-7 dias após o hCG. A SHO tardia é induzida pela gravidez, ocorrendo em cerca de 12-17 dias após o hCG, e é desencadeada pelo hCG endógeno produzido pelo tecido embrionário, principalmente em gravidezes múltiplas, ou com a administração de hCG para o suporte da fase lútea. A forma tardia apresenta mais frequentemente formas severas.
QUADRO CLÍNICO E TRATAMENTO
As manifestações clínicas da SHO refletem a extensão de extravasamento de líquido para terceiro espaço e consequente hemoconcentração. Os sintomas variam desde leve desconforto abdominal pelo aumento dos ovários ate insuficiência renal aguda e morte por trombose ou falta de perfusão de tecidos. Existem diferentes classificações da SHO, de acordo com dados clínicos e laboratoriais (Quadro 10-1).
QUADRO 10-1. CLASSIFICAÇÃO DA SÍNDROME DA HIPERESTIMULAÇÃO OVARIANA E TRATAMENTO
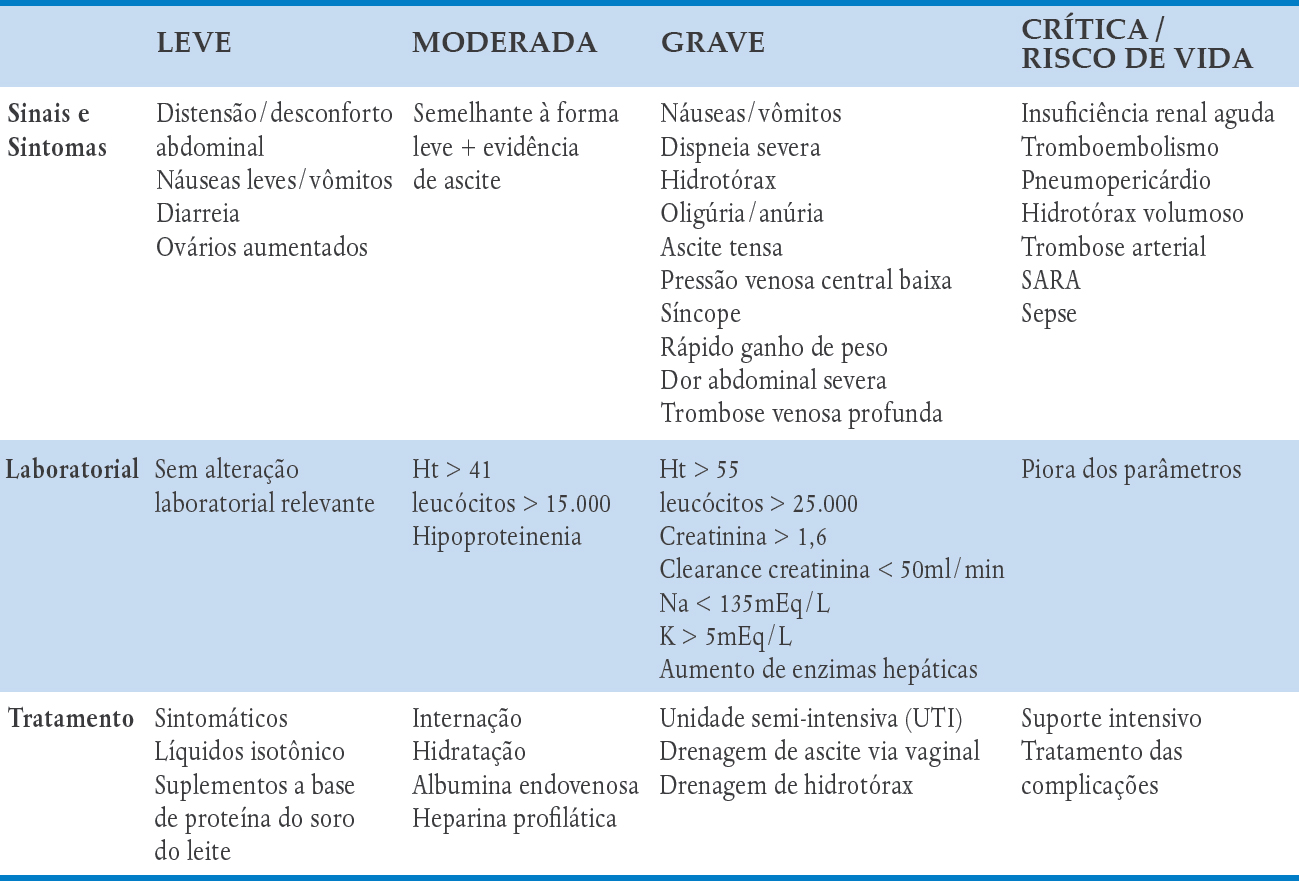
t: hematócrito; SARA: síndrome da Angústia Respiratória do Adulto. *Fiedler & Ezcurra. Reprod Biol Endocrinol. 2012 Apr 24;10:32.
Uma vez instalada a SHO, não conseguimos tratar a sua causa e devemos atuar no sentido de minimizar os sintomas e controlar suas consequências, o que muitas vezes tem que ser realizado por um profissional com experiência na área de reprodução humana.
Quando suspeitada, devem ser pedidos:
• hemograma;
• sódio/potássio;
• ureia/creatinina;
• albumina;
• ultrassom pélvico e abdominal, para avaliar os ovários e quantificar a ascite.
Quadros leves não necessitam de internação, mas é preciso manter contato constante com a paciente, ao menos por telefone. Deve-se estar alerta a dispneia e desconforto abdominal e orientar peso e medida da circunferência abdominal diários. A paciente deve ter acesso fácil e rápido ao seu médico sempre que precisar, pois as maiores iatrogenias são decorrentes de atendimentos emergenciais em prontos-socorros por médicos que, por não atuarem na área de reprodução humana, não sabem como lidar com a SHO.
Medidas terapêuticas incluem:
• repouso, pois com os ovários aumentados há maior risco de torção. Não se deve orientar restrição ao leito pelo risco de tromboembolismo;
• sintomáticos (analgésicos e antieméticos), se necessários;
• estimular ingestão líquida, preferencialmente de isotônicos;
• suplementos à base de proteína do soro do leite (para aumentar o aporte proteico).
Quadros moderados requerem internação, durante a qual devem ser pedidos diariamente os exames anteriormente citados, assim como medida de peso e balanço hídrico. Clearance de creatinina e enzimas hepáticas devem ser solicitados também. Entre as medidas recomendadas, estão:
• hidratação com soro glicosado 5% em volume necessário para manter diurese maior que 20-30 ml/h e reverter a hemoconcentração. O objetivo primordial é controlar hipotensão e oligúria, embora contribua para o aumento da ascite;
• albumina 25%: 50-100 mg em 4 horas, sendo repetidas de 12/12h a até, no máximo, de 4/4h;
• heparina profilática, pelo risco de eventos trombóticos pela hemoconcentração associada a repouso. O esquema mais utilizado é enoxaparina 40 mg subcutâneo ao dia;
• paracentese: indicada quando ascite volumosa cursa com dificuldade ventilatória, muito desconforto abdominal ou oligúria não responsiva a hidratação/albumina. Deve ser guiada por ultrassom e normalmente se usa a via vaginal. Em alguns casos deve ser feita repetidamente, até a resolução do quadro;
• toracocentese: em casos de ascite volumosa é comum hidrotórax, principalmente à direita, que normalmente se reduz após paracentese. Em caso de manutenção da dispneia e hidrotórax, deve-se proceder a toracocentese;
• diuréticos: furosemida 20 mg EV pode ser considerado após restauração do volume intravascular (hematócrito < 38%). Utilizar prematuramente ou em excesso pode agravar a hipovolemia e a hemoconcentração, aumentando os riscos.
Casos graves necessitam de internação em unidade semi-intensiva ou UTI. Complicações requerem tratamentos específicos, como correção de hiperpotassemia, drogas vasoativas quando falência renal e anticoagulação terapêutica em casos de trombose.
Apesar de autolimitada, casos extremos podem levar ao óbito. Mesmo formas moderadas e leves são muito traumáticas e desgastantes, tanto para a paciente como para o médico. Assim, hoje em dia, uma das maiores preocupações da RA é eliminar a SHO, por meio de medidas que previnam a sua ocorrência.
PREVENÇÃO DA SHO
Existem diversas maneiras de prevenir a SHO, aplicáveis antes de se iniciar a estimulação ovariana, durante a indução e após a coleta dos óvulos.
Antes da indução ovariana
A primeira medida preventiva da SHO é reconhecer as pacientes de risco para o desenvolvimento da síndrome e, nestes casos, individualizar o protocolo de indução da ovulação (Quadro 10-2). Existem fatores de risco bem estabelecidos, como baixo IMC, pacientes jovens, portadoras de Síndrome dos Ovários Policísticos e com história prévia de SHO. Provas de reserva ovariana, como contagem de folículos antrais (do 2º – 5º dia do ciclo) e dosagem de hormônio antimulleriano, podem ser úteis pra discriminar as pacientes de risco. Frente a esses fatores de risco primários, deve-se dar prioridade à utilização de protocolo curto com antagonista com baixas doses de gonadotrofinas (75-150 UI/ dia). Protocolos com antagonista têm menor incidência de SHO, além de permitir substituição do hCG para o trigger final da ovulação por agonista do GnRH, o que praticamente exclui a chance de SHO.
QUADRO 10-2. FATORES DE RISCO PARA A SÍNDROME DA HIPERESTIMULAÇÃO OVARIANA
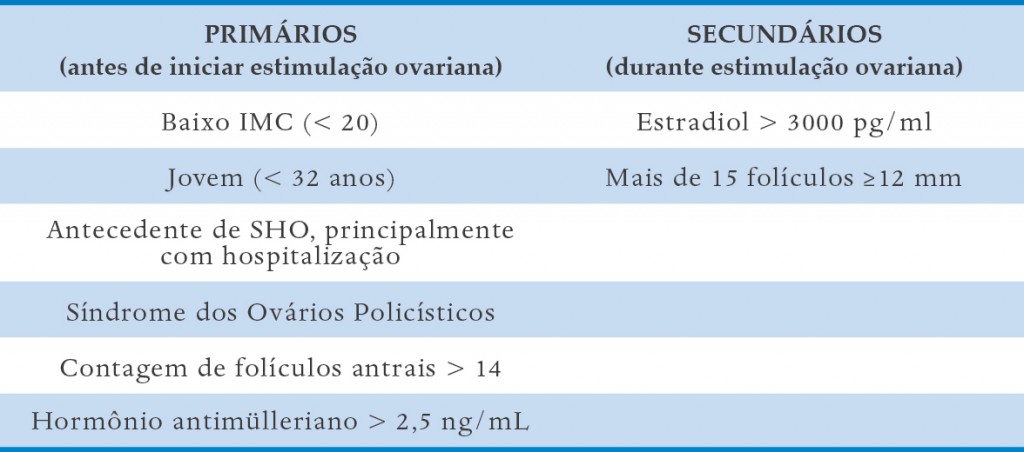
Durante a indução ovariana
Uma vez iniciada a indução ovariana, alguns parâmetros podem indicar um risco elevado à SHO, os chamados fatores de risco secundários (Quadro 10-2). Entre eles, altos níveis de estradiol e grande número de folículos, principalmente quando associados. Níveis de estradiol > 3000 pg/ml combinados com a contagem de mais de 15 folículos maiores que 12 mm no dia do agendamento da punção são preditores para SHO.
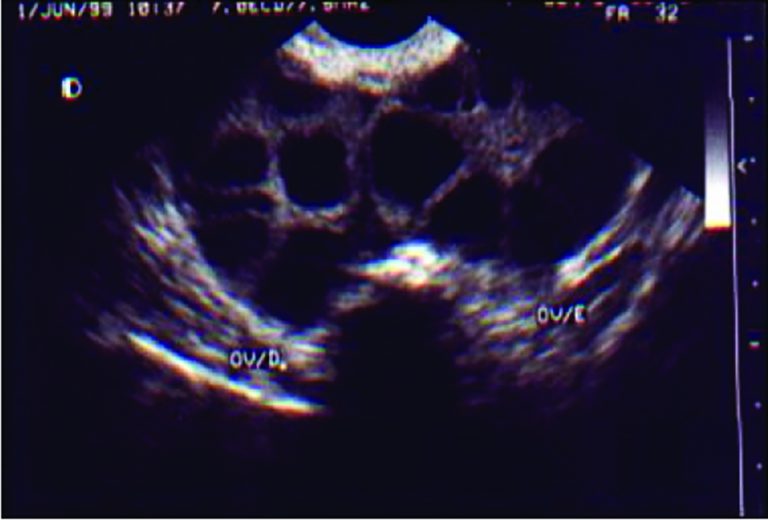
A imagem ecográfica típica é de ovários aumentados de tamanho, com múltiplos folículos com aspecto em “roda-de-carroça” e sinal de “kissing ovaries” (ovários se tocam ao centro) (Figura 10-1).
FIGURA 10-1. ULTRASSOM TRANSVAGINAL SUGESTIVO DE SÍNDROME DA HIPERESTIMULAÇÃO OVARIANA
Frente a esses fatores secundários, as seguintes medidas podem ser estabelecidas:
Coasting: consiste na parada temporária da administração de gonadotrofinas, mantendo o agonista ou antagonista do GnRH, e postergação na realização do hCG. Acredita-se que isso leve à apoptose dos folículos menores. Resultados melhores são obtidos quando o folículo maior já atingiu 16 mm e o hCG é feito quando o estradiol cair para 3000 pg/ml, não devendo ultrapassar três dias sem FSH. Apesar de ser efetivo para a redução dos níveis de estradiol, está relacionado a menores taxas de gravidez.
Cancelamento do ciclo: seria a forma mais eficaz de prevenir o agravamento da síndrome, entretanto, é emocional e financeiramente estressante para a paciente e deve ser reservado apenas para casos extremos.
No dia do hCG
No dia do hCG, se a paciente apresentar fatores de risco, como estradiol > 3000 pg/ml, mais de 15 folículos ≥ 12 mm ou sinais de ascite (mesmo discreta), três medidas podem ser tomadas:
Em protocolo curto com antagonista: substituir hCG para o trigger final por agonista do GnRH. Podem ser utilizados triptorrelina 0,2 mg, buserelina 0,5 mg ou leuprorrelina 1 mg em dose única subcutânea. O momento de realizar e o horário da coleta seguem os mesmo critérios utilizados com o uso do hCG. O agonista induzirá um pico endógeno de LH suficiente para a maturação oocitária final e a ovulação, entretanto este pico é mais efêmero e leva a bloqueio hipofisário posterior, com supressão dos níveis de LH endógeno, o que gera uma insuficiência lútea com consequente impacto na receptividade endometrial. Com isso, apesar de não interferir na quantidade de oócitos captados, taxa de fertilização e qualidade embrionária, há uma queda importante na taxa de implantação e gravidez nesses casos. Alguns pesquisadores sugerem um suporte de fase lútea mais agressivo, entretanto, o mais recomendado é a vitrificação dos embriões e a transferência num próximo ciclo.
Agonista dopaminérgico: estudos in vitro e em animais demonstraram dois mecanismos pelos quais esses medicamentos poderiam ser úteis na SHO. Eles agem nos receptores de VEGF, provocando sua internalização e impedindo, assim, a ação desse fator sobre ele; e levam também à redução na fosforilação desses receptores, etapa importante para o processo de aumento de permeabilidade vascular provocado pelo VEGF. O esquema mais utilizado é o uso da cabergolina (agonista da dopamina) na dose de 0,5 mg/dia por oito dias iniciando no dia do hCG, de preferência algumas horas antes de sua aplicação. Mais recentemente, foi sugerido o uso da quinagolida, que tem menor custo, entretanto alto índice de intolerância (náusea, vômito, sonolência). Outra opção é o uso de bromocriptina, que também tem alto índice de intolerância gástrica, sendo sugerido seu uso via retal (2,5 mg/dia por 16 dias). Ressaltamos que agonistas dopaminérgicos demonstraram eficácia na prevenção e tratamento somente da forma precoce da síndrome.
Pioglitazona: é um hipoglicemiante oral que mostrou uma ação nos ovários levando a uma menor produção de VEGF pelas células da granulosa. Estudos em humanos na prevenção da SHO ainda são limitados. Em 2011, estudo realizado no IPGO, apresentado no 6th World Congress on Ovulation Induction (Nápoles, 2010), demonstrou redução na incidência e gravidade da SHO com o uso de pioglitazona. Recomenda-se o uso de 30 mg/dia via oral, iniciando no dia do hCG por sete dias. Com seu uso, é observada uma queda importante do nível do estradiol sérico, que muitas vezes deve ser suplementado.
Durante a coleta de óvulos
Durante a captação oocitária, o uso profilático de soluções coloides pode ter efeito benéfico na prevenção da SHO, por aumentar a pressão oncótica intravascular e, com isso, reverter o extravasamento de líquidos para o terceiro espaço, além de se unir a mediadores responsáveis pela síndrome. Recomenda-se Albulmina 20% 50 ml ou Hidroxetilamido 6% 1.000 ml via endovenosa durante a coleta de óvulos.
Após a coleta de óvulos
Durante a fase lútea, em pacientes de risco, em primeiro lugar, não se deve usar hCG para suporte. Além disso, duas medidas podem ser úteis:
Criopreservação de todos os embriões com transferência em ciclos posteriores: isso é necessário se usou-se análogo do GnRH para trigger, mas mesmo com o uso do hCG é uma medida útil, pois impede que uma possível gestação agrave ainda mais o quadro de hiperestímulo, o que traria consequências dramáticas. Além disso, essa medida é sensata no sentido de que pacientes com SHO têm níveis suprafisiológicos de estradiol, que pode ser deletério para o endométrio e embriotóxico.
Antagonista de GnRh na fase lútea: recentemente, tem sido sugerido que antagonista do GnRH pode ter um efeito direto no ovário, diminuindo a produção de VEGF, além de suprimir as gonadotrofinas endógenas, que estimulariam os ovários. Estudos pequenos sugerem que seu uso durante a fase lútea em pacientes com risco elevado para SHO reduz incidência de casos graves e traz recuperação mais rápida. A dose recomendada é de 0,25 mg/dia por três dias, iniciando no dia da transferência.
QUADRO 10-3. MEDIDAS PARA PREVENIR A SÍNDROME DA HIPERESTIMULAÇÃO OVARIANA
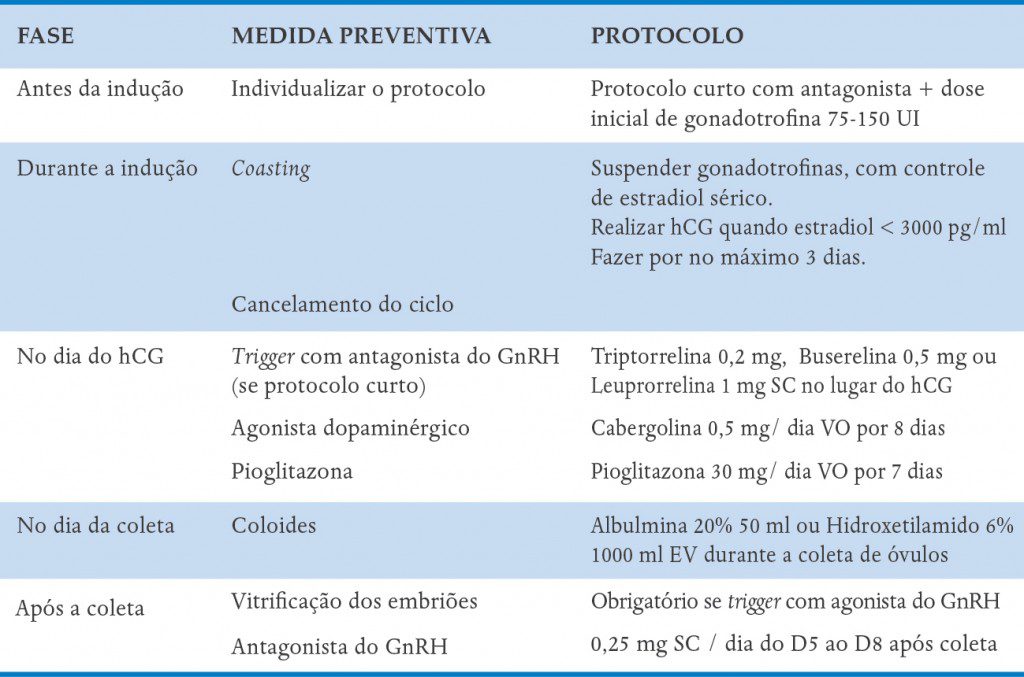
CONCLUSÃO
Os estudos relacionados à SHO têm permitido grandes avanços, que vão desde o aprimoramento farmacológico dos indutores da ovulação até o entendimento da fisiopatologia da enfermidade, seu tratamento e prevenção. Individualizar cada mulher e saber manusear a função ovariana é uma arte, e para dominá-la é preciso estar em constante atualização. O grande foco do especialista em reprodução assistida é maximizar as chances de sucesso, minimizando a morbidade e os riscos. Isso inclui a eliminação da SHO da prática clínica, o que hoje é factível com as diferentes linhas de prevenção.
Uma sequência lógica e segura é:
1. avaliar os fatores de risco antes da indução e, se presentes, utilizar protocolo curto com antagonista de GnRH e dose baixa de gonadotrofina;
2. se houver fatores de risco secundários durante o estímulo, optar pelo uso de análogo do GnRH para trigger no lugar do hCG;
3. se necessário, iniciar cabergolina ou pioglitazona;
4. aplicar albumina endovenosa durante a coleta;
5. fazer a vitrificação dos embriões.
Com essa sequência, a chance de ocorrência da SHO é mínima, mas, na eventualidade de acontecer, o médico deve estar bem preparado para conduzir adequadamente o quadro e reduzir ao máximo as complicações
